分子生理学研究室
担当教員/浅野 真司・波多野 亮
消化管では胃酸の分泌や、小腸における糖・アミノ酸などの栄養分の吸収、小腸・大腸におけるさまざまなイオンの分泌、吸収が行われます。また、腎臓では糸球体での血液濾過に引き続いて、尿細管での水や栄養分の再吸収、薬物などの分泌による排泄が行われます。このように、私たちの体の中では、日夜、上皮細胞を介した物質の輸送(分泌・吸収)が活発に行われており、精緻なバランスのもとに健康が維持されています。もし、消化管や腎臓の膜輸送タンパク質に異常が生じたり、機能調節のバランスが崩れると病気となります。本研究室では、消化管や腎臓における膜輸送タンパク質の生理的な機能調節メカニズムの解明や、新たな薬の作用点の発見を目指して、モデル動物(遺伝子操作を行った動物など)や培養細胞を用いた研究を行っています。

膜輸送タンパク質に対する遺伝子組換えマウスの行動観察
ゲノム機能学研究室
担当教員/稲津 哲也
患者さん由来のゲノム(全遺伝情報)の構造と情報の異常を解析し、どうしてそれらの異常にて病気を引き起こすのかを解析します。それらの結果を通じて、最終的に薬などの治療法を見いだしたり、予防に役立てたいと考えています。具体的な疾患として、尿酸代謝、先天代謝異常、早老症、精神遅滞等の研究を行っています。対象としては、分子から、細胞、個体、集団まで扱う予定でおります。
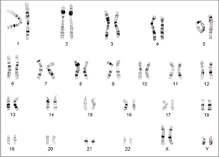
ヒト染色体(異常例)
生体情報制御学研究室
担当教員/鈴木 健二・河野 貴子
ヒトをはじめとした「多細胞生物」は細胞間の情報交換によって様々な生理機能を制御・調節しています。ホルモンや神経伝達物質などが伝える情報や刺激は細胞表面の受容体を介して様々な応答(増殖や分化、細胞機能の調節など)を引き起こしますが、そこには多くのタンパク質が関与することが知られています。細胞内情報伝達系といわれるタンパク質のネットワークは生物個体の恒常性の維持に重要な役割を果たしているばかりでなく、その破綻や異常が多くの疾患の原因となっていることがわかってきました。本研究室では、遺伝子工学的な手法を用いて肥満や糖尿病などの疾患の発症に関わる情報伝達分子のネットワークを分子レベルで明らかにして、それら疾患の新しい治療薬の開発に寄与することを目指しています。

研究室の風景
細胞工学研究室
担当教員/高田 達之
生殖細胞(卵子、精子)は我々の身体を構成する体細胞とは異なり、次世代へ遺伝情報を混合し、伝達するという目的のために分化した特殊な細胞です。生殖細胞は発生の極めて初期にその運命決定がなされ、体細胞とは異なる特有の細胞分裂、減数分裂を経て形成されます。この過程で遺伝情報は染色体の組換えと組合せにより多様性を獲得します。こうして生殖細胞にゆだねられた遺伝情報は有性生殖により新たな世代をつくりだしてゆきます。我々はマウスおよび霊長類ES、iPS細胞を使用して、化学物質が生殖細胞分化に与える影響とそのメカニズムを遺伝子発現とDNAメチル化に注目して研究しています。また、琵琶湖固有魚種を用いたin vitroでの生殖細胞分化、配偶子形成による保存研究およびトランスクリプトーム解析を利用した性分化に関する研究も行っています。
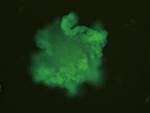
非ヒト霊長類ES細胞の分化と生殖細胞マーカーの発現
神経化学研究室
担当教員/谷浦 秀夫
脳は知覚の入力、運動の出力および記憶学習といった高次機能を担っている複雑な組織です。これらの脳の機能を主に司っているのがニューロンと呼ばれる神経細胞です。ニューロンは、長い神経突起を伸ばした特殊な細胞で、ニューロン同士がお互いにシナプスと呼ばれる構造を介して情報を伝達する神経回路を形成することによって機能しています。神経化学研究室では、ニューロンの発達過程で過剰なニューロン死や突起伸展異常が認められる神経発達障害疾患プラダーウィリ症候群と中年から高齢者で原因不明のニューロン死が起こり記憶障害などの認知症となる神経変性疾患であるアルツハイマー病の発症病態機構の解明をめざして研究を行っています。ニューロンに分化誘導できる細胞や直接ラット脳より取り出したニューロンといった培養神経細胞を用いて研究を進めています。

胚性がんP19細胞より分化したニューロン(赤)
感染制御学研究室
担当教員/土屋 友房・山田 陽一
世界保健機関(World Health Organization: WHO)の統計によると、人類の死亡原因の第一位は微生物感染症です。先進諸国では、抗菌薬が効かない耐性菌(特に多剤耐性菌)(微生物)による感染症が大きな問題になっています。私達は「耐性菌による感染を制御し耐性菌を制圧する」という夢を持ちChallenge しています。この夢を実現するため、次の三つの戦略を考え研究を進めています。1)耐性菌の耐性系を解析してその性質と弱点を明らかにする(敵を知る)、2)抗菌薬の適正使用により耐性菌を出現・拡大させない(敵を生まない・増やさない)、3)耐性菌に有効な医薬品の開発(敵を叩く)、の三つです。これまでの研究により、これらの点について大変興味深い基礎データが得られています。
臨床薬理学研究室
担当教員/服部 尚樹
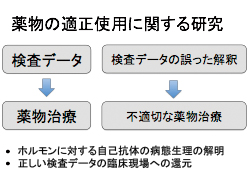
「検査」は疾患の薬物治療方針を決定する上で極めて重要です。しかし、もし検査結果が誤って解釈されると「誤診」につながり、不適切な薬物治療や不要な検査がなされ、患者さんにとって不幸な結果をもたらします。
本研究室では、種々のホルモンに対して自己抗体が出来ることを明らかにし、その病態生理の解明を行っています。脳下垂体から分泌されるプロラクチンや甲状腺刺激ホルモン、膵臓から分泌されるインスリンに対する自己抗体が出来る人がいます。自己抗体が出来ると、ホルモンの生物作用は弱くなる一方で、血液中のホルモン値は上昇します。このため、この病態を知らないと、例えばプロラクチンを産生する下垂体腺腫と誤診され、副作用の多い薬を長期間服用し、手術にまで至る症例があります。このプロラクチン自己抗体による「マクロプロラクチン血症」は全国から検査の依頼が本研究室に来ており、正しい検査結果を臨床現場に還元しています。
免疫系‐神経‐内分泌相互作用
情報薬理学研究室
担当教員/藤田 典久・齋藤 僚
ホルモンや成長因子、神経情報伝達物質などさまざまな生体内物質が細胞表面の受容体に働きかけ、生命体は恒常性を維持していますが、それらの作用の過不足は重篤な疾患をもたらします。市場に出ている医薬品の多くは受容体を標的としていることから、本研究室ではin vitro、in situの実験に加え、コンピュータを用いたシミュレーションや生命情報学的解析を行い、医薬品と受容体の相互作用と薬効メカニズムを分子レベルで解明し、その結果を創薬に生かすことを目的としています。
最近は、ゲノム解析から存在が明らかにされた『みなしご受容体(オーファン受容体)』に注目し、それらを活性化する生体内物質を見つけることを手がけています。すでに3つのオーファン受容体について刺激物質を発見しましたが、まだその生体内での意義については明らかになっていません。当面は、これらオーファン受容体とその刺激物質の生理的な意義を解明することに焦点をあて研究を進める方針です。

神経発生システム研究室
担当教員/小池 千恵子
私たちは、毎日の生活における認識や行動の多くを視覚情報に依存しています。網膜は光情報を神経情報に変換する唯一の神経組織です。視覚については、大脳皮質視覚野で情報処理が行われることはよく知られていますが、網膜で基本となる重要な情報処理が行われています。本研究室は、網膜の情報処理の中心となるON・OFF回路を生体工学を用いて解析することにより、網膜回路による視覚応答制御の解明を目指します。
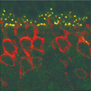
網膜双極細胞において視覚伝達チャネルTRPM1(赤)はグルタミン酸受容体mGluR6(緑)と共局在している
分子薬効毒性学研究室
担当教員/藤田 隆司
私たちの研究室では、骨の作られ方、骨の維持について研究しています。研究の最大目標は、骨粗鬆症のような骨が弱くなる病態生理を理解し、最適な治療戦略を開発することです。骨の強さが失われるメカニズムを細胞・分子・遺伝子の働きを評価することで、治療方法を開発しようと試みています。骨粗鬆症は、骨形成担当細胞前駆細胞の分裂とアポトーシスによる細胞死のスピードのバランスが崩れることで、異常に骨形成担当細胞の数が減少するため起こります。研究テーマの中心は、骨の老化に伴う酸化ストレスの蓄積のような原因の探索、遺伝病・骨代謝性疾患の病態的変化、薬の効果等を調べることです。「健康な骨」が作られるために必要な分子基盤を確立したいと考えています。
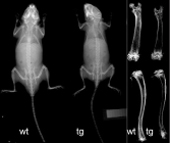
遺伝子改変動物のX線像 (左:全身像、右:摘出長管骨) 遺伝子改変動物(tg)は野生型(wt)に比べて骨量が低下している。









