体内時計の精度はタンパク質に内蔵されていた―シアノバクテリアの時計の本質を解明―
研究成果のポイント
- 体内時計の「環境に左右されない正確さ」が、タンパク質の時計に内蔵されていることを実証
- 20種類以上の時計タンパク質「KaiC」の周期変異体を使って、細胞内と試験管内の両方で高い周期精度を確認
- 細胞内では細胞環境が地球環境に合わせてわずかに周期を微調整している可能性が示唆され、人工的な生物時計の設計や、生物時計の精密な時間制御技術の開発につながる可能性に期待
概要
大阪大学大学院理学研究科(名古屋大学高等研究院 客員研究員)の伊藤(三輪)久美子特任助教、関西医科大学医学部の岡野(今井)圭子講師、立命館大学生命科学部の寺内一姫教授、名古屋大学の故近藤孝男特別教授の研究グループは、シアノバクテリア(光合成を行う細菌)の体内時計の「環境に左右されない正確さ」が、タンパク質の時計に内蔵されていることを実証しました。
生物は地球の自転に伴う昼夜の環境変化に適応するため、約24時間周期で振動する体内時計の仕組みを備えています。体内時計は気温や光の強さなどの環境が変わっても、その周期はほとんど変わらず、非常に高い精度で保たれることが知られています。
シアノバクテリアの体内時計は試験管内で再現することができ、研究グループは、「生きた細胞内でのリズム」と「試験管内で再現したタンパク質時計のリズム」の性質を詳しく解析しました。そして、時計の精度が「KaiC」という単一のタンパク質の性質に本質的に組み込まれていることを明らかにしました。
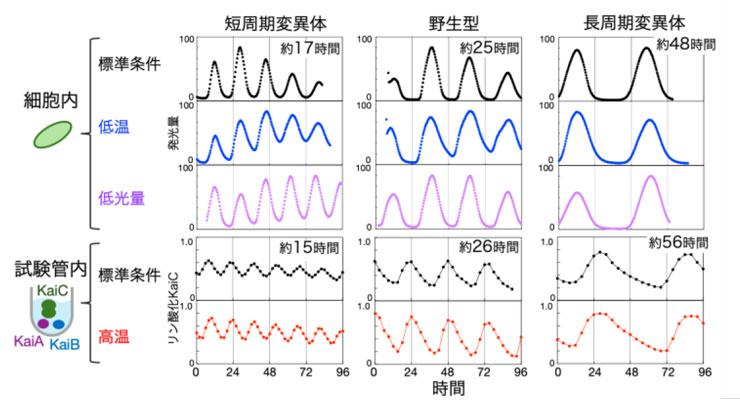 図1.KaiCの周期変異体の細胞内と試験管内のリズム(代表例)
図1.KaiCの周期変異体の細胞内と試験管内のリズム(代表例)
温度や光量が変わっても、野生型(通常のタイプ)・短周期および長周期変異体の体内時計の周期は、ほとんど変化しない。さらに、細胞内の時計の周期は試験管内の時計の周期に比べて、短周期変異体は長く、長周期変異体は短くなり、地球の自転周期にわずかに近づく傾向がみられる。
本研究成果は、「生命が時間を刻む仕組み」の本質的な理解を大きく前進させるものです。本研究成果は、米国科学誌「Proceedings of the National Academy of Sciences of the United States of America(PNAS)」に、3月17日(火)午前4時(日本時間)に公開されました。
大阪大学大学院理学研究科 伊藤(三輪)久美子特任助教のコメント
本研究は、約25年にわたり、故近藤特別教授の研究室でこつこつと積み重ねてきた成果です。実験で、シアノバクテリアの細胞内や試験管内のとてもきれいなリズムを見るたびに、1ミリメートルの 500分の1程度しかない小さな微生物の中に、これほど正確な時計を生み出す仕組みがあるという事実に、いつも驚かされます。
研究の背景
ヒトや植物、バクテリアまで、多くの生物は体内時計によって生命活動を約24時間周期で調節することで、地球の自転による昼夜の環境変化に適応しています。心拍や細胞分裂など一般的な生体リズムでは、温度や環境が変わると周期も変化します。しかし体内時計は、気温や光の強さなどの環境が変わっても周期がほとんど変わらず、非常に高い精度で保たれることが知られています。
光合成を行う原核生物であるシアノバクテリアも体内時計の仕組みを持っています。興味深いことに、シアノバクテリアの体内時計は試験管内で再現することができ、3つの時計タンパク質KaiC,KaiA,KaiBを試験管の中で混合すると、KaiCタンパク質のリン酸化※1と呼ばれる活性が約24時間周期のリズムを示します。最も重要なのはKaiCで、KaiCの酵素活性※2によってリズムの周期が決まることです。しかし、生きた細胞の中では、これらのタンパク質に加えて遺伝子の働きなども関与します。そのため、シアノバクテリアの時計の正確さを本当に決めているのは、タンパク質そのものなのか、それとも細胞全体の仕組みなのかという問いが長年残されていました。
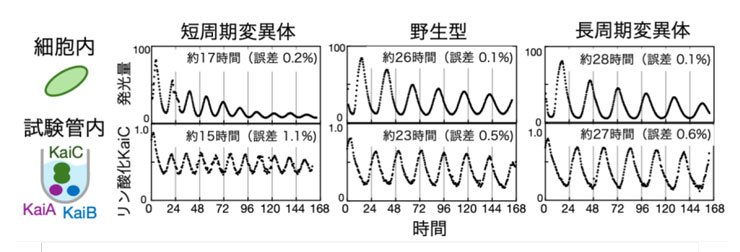 図2.細胞内と試験管内のリズムの周期は高精度
図2.細胞内と試験管内のリズムの周期は高精度
体内時計の周期は1周期ごとのばらつき(誤差)が0.1から1%程度と、極めて正確。
研究の内容
研究グループは体内時計の周期が15時間から60時間まで大きく異なる20種類以上のKaiCの変異体を用い、「生きた細胞内でのリズム」と「試験管内で再現したタンパク質時計のリズム」の性質を詳しく調べました。その結果、温度や光の強さ、細胞内の代謝状態が変化しても、変異体の周期の長さはほとんど変わらないことを明らかにしました(図1)。
また、多くの非概日性の生体リズムでは、周期に数%から数10%程度のばらつきが報告されています。これに対し、本研究で解析した時計の周期は、細胞内でも試験管内でも、ばらつきが0.1〜1%程度という極めて高い精度で維持されていることも分かりました(図2)。この性質は周期が短い変異体でも長い変異体でも共通しており、変異体の周期の長さに関わらず、「環境に左右されない周期の正確さと精度」は時計の基本設計として備わっていることが示されました。
一方で、試験管内の時計と細胞内の時計を詳しく比較すると、「細胞内の時計の周期は試験管内の時計の周期に比べて、地球の自転周期にわずかに近づく傾向」がみられました(図1)。これは、細胞内の仕組みが時計の周期をわずかに調整し、より地球環境に適した時間に近づけている可能性を示唆しています。
KaiCは、細胞の中でエネルギーとして使われるATPという物質を、ゆっくり消費しながら動くタンパク質です。本研究では、このエネルギー消費の速さが、時計の進む速さと密接に関係していることも確認されました。これは、体内時計の正確さが細胞全体の複雑な仕組みによって生み出されているのではなく、単一タンパク質の分子レベルの性質として組み込まれていることを意味します。ただし、細胞内ではその関係がやや弱まり、細胞内の仕組みも周期の調整に関わる可能性が示されました。
これらの結果は、体内時計の周期の精度と環境非依存性が、KaiCタンパク質に内蔵された基本設計であることを示しています。
本研究成果が社会に与える影響(本研究成果の意義)
シアノバクテリアは、光合成により地球に酸素をもたらし、現在の生命環境の土台を築いた微生物であり、古くから体内時計を備えていたと考えられる生物です。その時計は、わずか3つのタンパク質だけで機能するという、極めて単純な仕組みです。
本研究は、この単純な時計が高い精度と環境非依存性を備える仕組みを明らかにしたものであり、多くの生物が持つ体内時計の普遍的な原理の理解につながる基礎的知見を提供します。さらに本成果は、人工的な生物時計の設計や、生物時計の精密な時間制御技術の開発につながる可能性があります。
論文情報
本研究成果は、2026年3月17日(火)午前4時(日本時間)に米国科学誌「Proceedings of the National Academy of Sciences of the United States of America(PNAS)」(オンライン)に掲載されました。
- タイトル:Intrinsic period stability of the cyanobacterial circadian oscillator across in vitro and in vivo conditions.
- 著者名:Kumiko Ito-Miwa*, Keiko Imai, Kazuki Terauchi, and Takao Kondo
(伊藤(三輪)久美子、今井 圭子、寺内 一姫、近藤 孝男) - 掲載誌:Proceedings of the National Academy of Sciences of the United States of America(PNAS)
- DOI:10.1073/pnas.2526714123
本研究は、大隅基礎科学創成財団、文部科学省 科学研究費助成事業(25H02446,23K25984,17H01427,15K21523,23K05031,17K19247,19K05833,24H02301,24K01686) の支援を受けて実施されました。
用語説明
- ※1 リン酸化タンパク質の決まった場所に「リン酸」という小さな化学物質が結合すること。KaiCはリン酸が結合したり離れたりする性質があり、その変化をゆっくりと繰り返すことで約24時間のリズムを生み出す。
- ※2 酵素活性タンパク質が化学反応を進めるはたらきのこと。KaiCに関しては、ATPというエネルギー分子をゆっくり分解するはたらきが、時計の進む速さを決めている。




