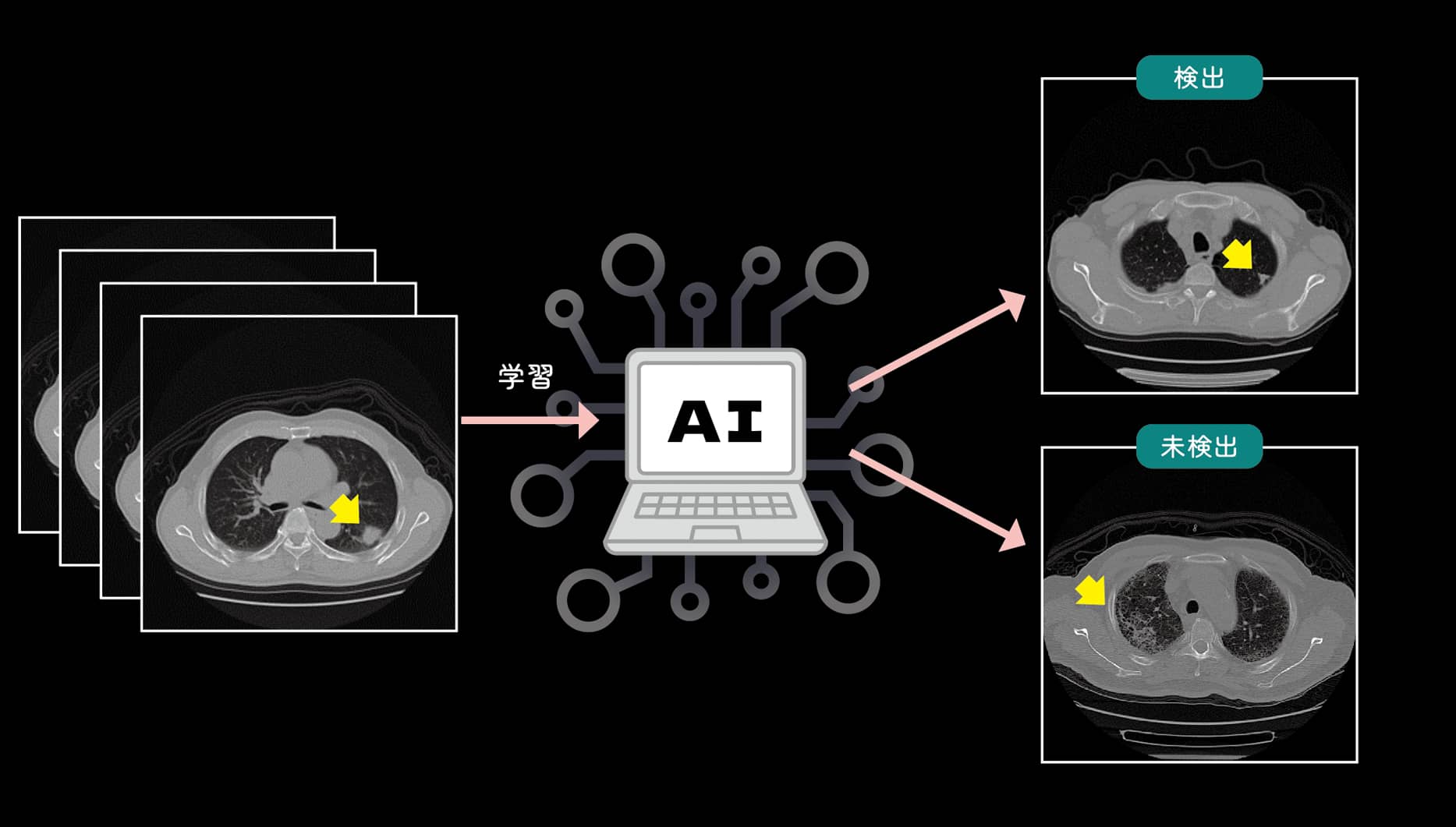
乳がんなどの検診では、マンモグラフィ検査などによる画像を元に専門の読影医が病状を判断している。このような検診の自動化、AIによる病変の自動検出に中山良平は挑戦している。それも単に画像から異変部を検出するのではない。いったん正常な場合の画像を想定し、その差分から異変を検出する。逆転の発想に基づく革新的な技術である。
医工連携の先駆け、課題はデータに
中山良平は工学部情報工学科から大学院の途中で医学系へ転じ、医工連携に取り組むようになった。そのきっかけを「大学1年生のときに小学校時代からとても仲のよかった友だちが、事故で下半身不随になりました。彼のために工学を使って何かできないかと考えたのがスタートです」と振り返る。
やがて大学4年生のときに、ある学会で乳腺専門医と出会う。この医師から工学の知見を活用する画像検診の可能性を教わり、自分の進む道が見えた。
その専門医、乳がんの世界では著名だった難波清氏が、医学領域における工学の可能性に目を開いてくれた。中山が医工連携の先駆けとして取り組んだテーマ、それはコンピュータ活用による乳がんの画像検診である。マンモグラフィの普及に伴って、乳がん検診の受診率が高まっていった。その結果、読影枚数が急増しつつあり、読影医にかかる大きな負担が問題となり始めていたのだ。
「コンピュータで画像検診をサポートできるようになれば、読影医の負担を少しでも軽減できます。ただ研究を進めるためには、マンモグラフィによる画像検診データが欠かせません。そこで修士2年から三重大学の医学系研究科に移りました」
データは得やすくなったものの、画像認識に関する指導教官がいなかった。そのため中山は、その頃すでに世界的な権威として知られていたシカゴ大学の土井邦雄教授に、メールで指導を依頼する。やがて土井教授に誘われてシカゴ大学に移り、最先端レベルの画像認識技術を学んだ。
研究テーマは病変部位の画像認識である。マンモグラフィ技術に関して世界で最も進んでいたアメリカでも、乳がん検診では3割程度の見落としがあるといわれていた。見落としを避けるため読影医には、より注意深い読影が求められる、すなわち読影医の負担はより大きくなる。読影医をサポートする技術開発への期待が、少しずつ高まり始めていた。
読影の結果、乳がんの可能性の疑われる患者には、針生検が行われる。これは比較的侵襲の少ない検査法とはいえ、針を刺されるダメージは、見た目に敏感な女性にとって大きな心理的負担となるケースもあった。
「針生検をすると乳房に傷痕が残ります。それを苦にして自ら命を断つ女性さえいる。なんとかしてそんな女性を救いたいのだ、と難波先生は話されていました。自分もなにか手助けをしたいと思い、早く研究を進めなければと励んできたのです」
中山は今のような画像関連のAIが誕生する前から、デジタルでの画像処理に取り組んできた。アナログ画像と比べてデータ量に限りのあるデジタル画像に対しては、偏見もまだ残っているような状況下での取り組みである。とはいえ先進国アメリカでは、すでに画像データセットも公開されデジタル診断への基盤が整備されつつあった。
異常画像ではなく、正常画像をベースに判断
「幸いにも2010年頃からはニューラルネットワークが進化し始め、画像診断に使えそうな機運が高まってきました。とはいえ人に使うためには、明確なエビデンスが求められます。一方でこの間にディープラーニングが凄まじい勢いで進化しましたが、そのエビデンスに懸念事項もあり今一つ信用できません。そのためあえてディープラーニングを使わずに論文を書いていると、査読者からディープラーニングを使ってやり直せとリジェクトされるケースもありました」
試行錯誤しながら研究を進めていた中山に、ある閃きから一大転機が訪れた。
「工業製品の検品などで活用されている異常検知を、乳がんの判定に応用できるのではないかと考えたのです。それまで取り組んでいた画像処理ベースの技術では、対象となる病変の画像特徴を学習させます。したがってこの技術では、学習した病変しか検出できません。実際には撮像したCT画像には、あらゆる病変が写されています。にもかかわらず学習した一つの病変しか検出できない技術では役に立たない。たとえば乳がんによる石灰化を学習させれば、その病変は見つけられても、腫瘤やFAD(局所的非対称性陰影)までは検出できなかったのです。なんとかしてあらゆる病変を検知できるアプローチはないか。いろいろ考えた末にたどり着いたのが異常検知だったのです」
工業用品における異常検知とは、正常な製品の画像を基準として、検品対象の画像を画像認識によって比較し、わずかな差異までも検出する手法だ。もとより従来のマンモグラフィ検診でも、読影医は異常部位を読み取ろうと画像をチェックしていた。ただ人の体は工業製品と異なり、そもそも正常画像が人により異なる。そのため異変のある画像を見ていても、それが異変なのかどうかを判断するのは決して簡単ではない。
「そこで発想を転換して、まずあらゆる患者さんの画像から、いったん正常な形を再現すればよいのではないかと考えたのです。再現された正常な画像、すなわちその患者さんにとって本来あるべき姿と実際の画像を比べてみる。この比較をすれば異変をより正確に判断できるはずです」
異変部位があるかどうかが不明な画像から異変を読み取るのではなく、その画像から本来あるべき正常な姿をいったん再現したうえで比較すれば、異変がより明確になる。独自の方法論は定まった。けれども、そこから先の道のりも決して平坦なものではなかった。
画像再生システムの進化
異常検知は、工業製品を対象として開発された手法であり、工業製品とは規格が厳密に定められたモノだ。したがってどこかに異常がある場合、正規品と比べてみればすぐにわかる。これに対して人の体はそうはいかない。そもそも乳房の形そのものが一人ひとり違う。だから乳がんの発生していない正常な人の画像を多数集めても、一人としてまったく同じ画像はない。しかも同じ人を対象としていても、撮像するたびに微妙な違いが出てくる。
「正常な形といっても、人の場合は工業製品のような単一規格ではありません。したがって正常にもバラエティがある前提で、モデルを構築する必要があります。そのため、まずある程度以上の画像を事前に学習させなければなりません。ただし学習させる枚数がひたすら多ければよいかといえば、そう単純な話でもありません。学習モデルに対する情報の与え方にもノウハウが求められるのです」
画像データを入力した段階で、正常な部分はそのまま復元する。同時に異常な部分は復元せずに、正常な構造に置き換えて復元する必要がある。そのため最初に取り組んだのがオートエンコーダー、すなわち入力データをいったん圧縮し、圧縮データから元のデータを復元する技術である。データ圧縮から復元に至る過程で異常な部分、つまりノイズを除去して再現しないようにする。
「ただこれだけでは、正常な部分がきちんと正常な形に復元できるけれども、異常もある程度復元されてしまいます。そこで次に取り組んだのが畳み込みニューラルネットワークを活用するVAE(Variational Autoencoder:変分オートエンコーダー)です。VAEでは入力情報をいったん正規分布に落とし込み、そこから復元します。正規分布に落とし込んだ段階で、異常な部分はデータから外されてしまいます。だからその部分を取り除いて復元すれば、異常な部分は再現されません」
地道にステップを踏んでいき、精度は少しずつ高まっていった。けれども、まだまだ決して満足できるレベルには到達できていなかった。読影医の代わりとして、実際に治療にあたる医師たちに納得してもらうためにはより高精細なモデルが必要だった。
ドクターに納得してもらえる画像生成へ
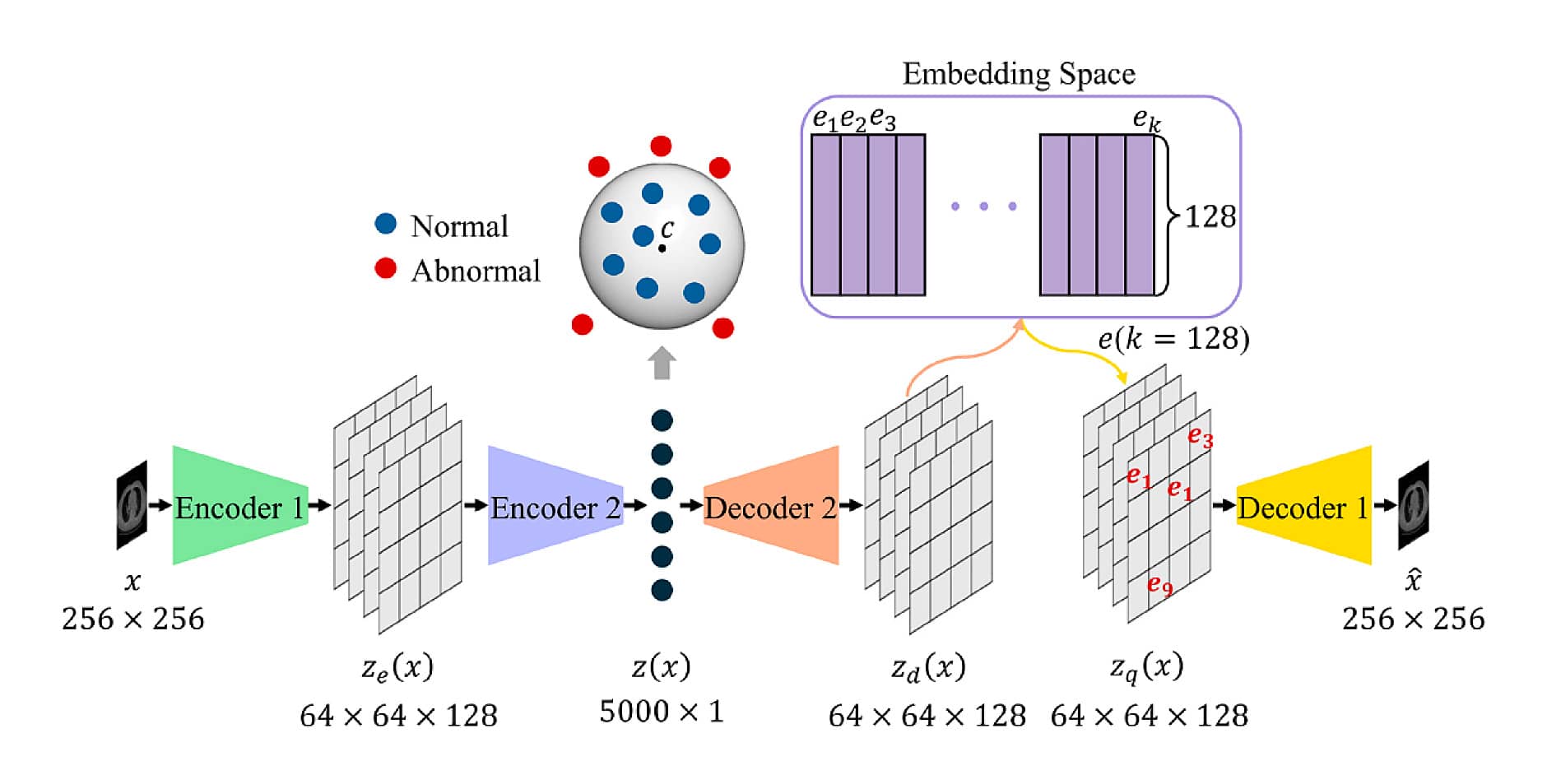
次に取り組んだのが、より高精細な再構成を実現するVQ-VAE(Vector Quantized-Variational Auto-Encoder:ベクトル量子化変分自己符号化器)だ。VAEが正規分布を活用したのに対して、VQ-VAEではベクトルを使う。
「ただしVQ-VAEは再構成能力が高いために、異常構造まで再構成してしまう点が問題として残ります。そこで異常検出に使われるSVDD(Support Vector Data Description:サポートベクトルデータ記述)も併用しました。SVDDを使えば、まず正常なデータポイントが表現されるので、そこから異常値を特定できるようになります。これにより異常な部分を再構成しないようにできます」
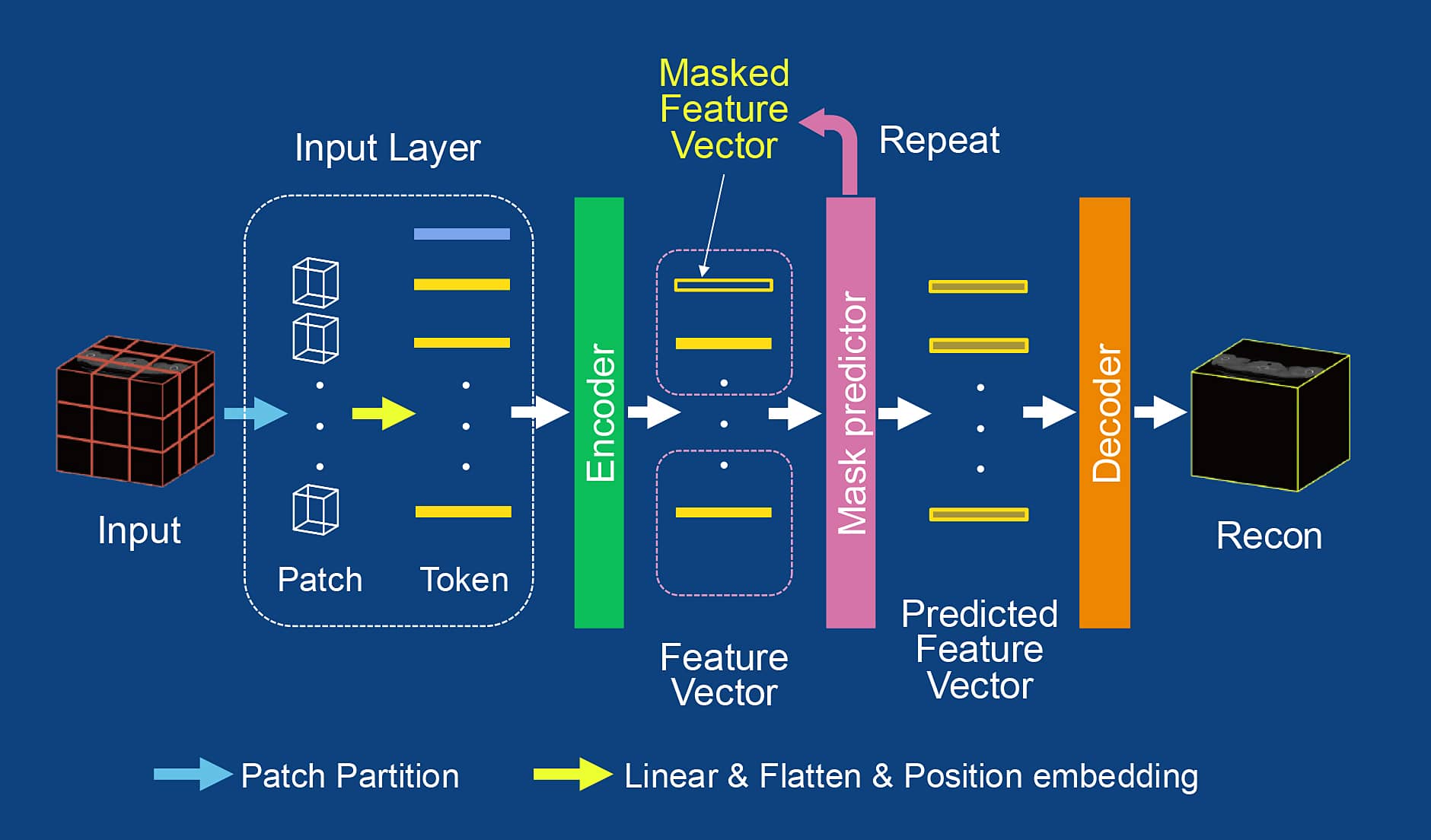
さらに精度を高めるために取り組んでいるのがビジョントランスフォーマー(Vision Transformer)と呼ばれる、深層学習モデルだ。これはChatGPTなど生成AIの自然言語処理で使われている技術を、画像認識に適用したものである。その結果、これまでよりも大域的な特徴を多様に捉え、画像の網羅的な学習が可能となる。
「ビジョントランスフォーマーを活用すれば、周囲の正常組織から異常部位の正常時の構造を予測できるようになります。これにより、医師に対してAIが異常と判断した根拠を示すことができるので、説明可能なAIとしての機能を果たせると期待されます」
ビジョントランスフォーマーを活用する技術については、いま特許申請が進められている。ただし、これにも満足せずに中山らはさらに、生成AIを活用する画像作成の新たなアプローチにも取り組んでいる。あくなき研究のゴールとして見据えているのは「ドクターが納得してくれる画像」だという。
「患者さんのデータを元に、この人が正常な状態だったらこうなりますねと、再構成した画像データをドクターに見せます。それと実際の画像を見比べたドクターから“なるほど、確かにここに異変があるな”と言ってもらいたい。比較すれば病変があるのかどうかがひと目でわかり納得もしてもらえる。そんな画像を作りたいのです」
そのためには、まだ研究を突き詰める必要がある。ゴールを100点満点とすれば、現状はまだ65点ぐらいというのが中山の評価だ。とはいえ、さらに点数を高めていくための道筋は、ある程度見えてもいる。乳がんに苦しむ女性を一人でも多く救うために、さらなる研究が続けられている。