空気中の酸素を用いる選択的合成 -連続四置換炭素を有するγ-ラクトンの合成-
概要
理化学研究所(理研)環境資源科学研究センター触媒・融合研究グループのフローリアン・ピュナー特別研究員(研究当時)、五月女宜裕専任研究員(研究当時、現客員研究員)(開拓研究本部袖岡有機合成化学研究室専任研究員(研究当時)、現立命館大学生命科学部教授)、袖岡幹子グループリーダー(開拓研究本部袖岡有機合成化学研究室主任研究員(研究当時))らの共同研究グループは、空気中の酸素を酸化剤として利用し、3位と4位に二つの連続四置換炭素[1]を有するγ-ラクトン[2]の合成を実現しました。
本研究成果は、酸素酸化反応による複雑な分子の選択的供給に貢献すると期待されます。
今回、共同研究グループは、空気中の酸素を用い、ラジカル[3]環化/酸素付加を鍵工程として、二つの連続四置換炭素を有し、さまざまな分子に変換できるγ-ラクトンの合成を実現しました。また、どのようにして主生成物を選択的に与えるかという仕組みを、計算化学を用いて明らかにしました。
本研究は、科学雑誌『Angewandte Chemie International Edition』オンライン版(6月20日付)に掲載されました。
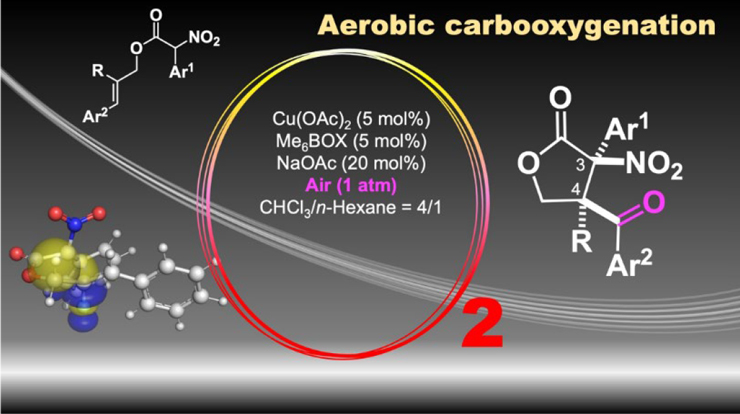 空気中の酸素を用いるγ-ラクトンの合成
空気中の酸素を用いるγ-ラクトンの合成
背景
酸化反応は、化学産業プロセスの30%以上を占める重要な反応です。空気中に豊富に存在する酸素はクリーンな酸化剤として注目を集めていますが、酸素は通常の状態では安定しているため、温和な酸・塩基条件において酸化剤として用いることは困難です。また、ラジカル反応の条件においては、酸素が活性酸素に変換されるため反応性の制御が難しく、その成功例は限定的でした。さらに、爆発の危険を避けるために、濃縮された酸素ではなく、空気中の酸素を活用することが望まれていました。
共同研究グループは、空気中の酸素を使い、二つの連続四置換炭素を有するγ-ラクトンの合成を目指しました。
研究手法と成果
五月女専任研究員らは、比較的寿命の長い持続性ラジカル[4]を用い、カテコールとの脱水素型クロスカップリングの開発を2020年に報告しました(図1-1)。また、従来エネルギー的に不利と考えられてきた吸熱型ラジカル付加(図1-1、工程i)が進行した後に、発熱的な酸化的芳香族化により進行するユニークな連続反応プロセスも明らかにしていました(図1-1、工程ii)注)。寿命が短い反応性ラジカル(短寿命ラジカル)[5]にも、この原理を応用することができれば、従来法では構築困難な新たな分子を合成することが可能になります。
共同研究グループは、反応性の高い三級炭素ラジカルと、ジェミナル二置換アルケン[6]とのラジカル環化を進行させた後、生じたベンジルラジカルを酸素により速やかに補足できれば、3位と4位に二つの連続四置換炭素を有するγ-ラクトンを合成できると考えました(図1-2)。
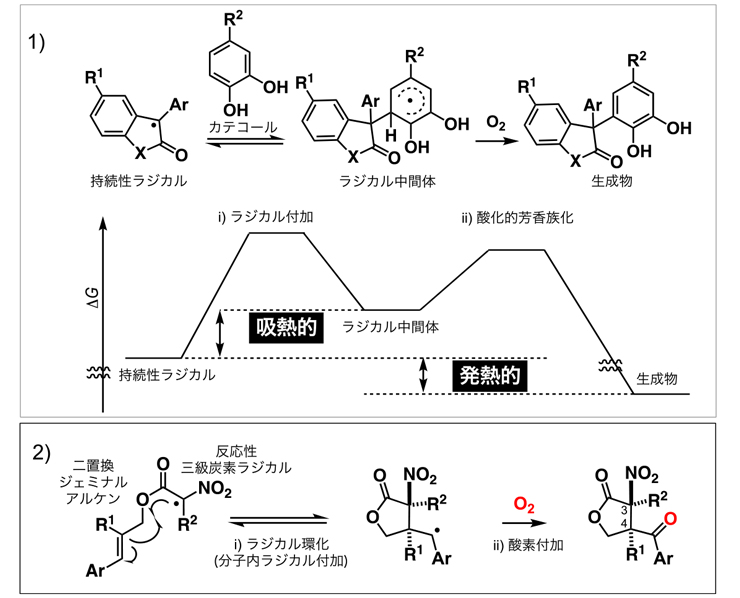 図1 ラジカルの吸熱的/発熱的連続反応を基盤とする酸化的分子変換
図1 ラジカルの吸熱的/発熱的連続反応を基盤とする酸化的分子変換
1)持続性ラジカルのカテコールへのラジカル付加/酸化的芳香族化。
2)反応性三級炭素ラジカルとジェミナル二置換アルケンの分子内ラジカル付加/酸素付加。ラジカル環化における1電子の動きは片矢印を用いて示す。
共同研究グループは、ラジカル前駆体としてニトロエステル、ラジカル受容体としてジェミナル二置換アルケンを有する「原料1a」を設計しました(図2)。空気中の酸素を酸化剤として、またクロロホルムとヘキサンの混合溶媒を用いた反応条件下、酢酸銅、Me6BOX配位子、および酢酸ナトリウムは触媒として機能し、ラジカル環化/酸素付加が進行し、所望の連続四置換炭素を有するγ-ラクトン2a(2は生成物の化合番号)が得られることを見いだしました。また、ニトロ基とベンゾイル基が同一方向に配置されたsyn体とこれらの官能基が反対方向に配置されたanti体が生じる可能性がありますが、本反応では高い選択性でsyn体が得られました。
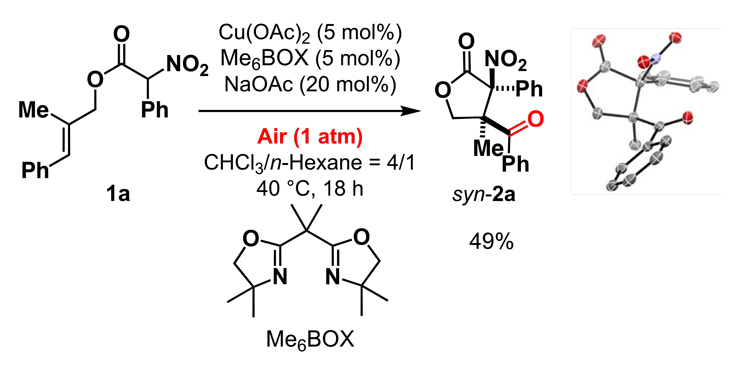 図2 空気中の酸素を酸化剤として用いた反応条件の確立と生成物の構造決定
図2 空気中の酸素を酸化剤として用いた反応条件の確立と生成物の構造決定
2aの結晶構造解析により、生成物の相対立体配置は、ニトロ基とベンゾイル基が同一方向に配置されたsyn体であると決定した。
さらには、この反応条件では、Rとして炭素鎖を有する「1b-1g」に加えて(図3-左)、フッ素(F)を有する原料「1h-1m」もγ-ラクトン2へと変換できました(図3-右)。
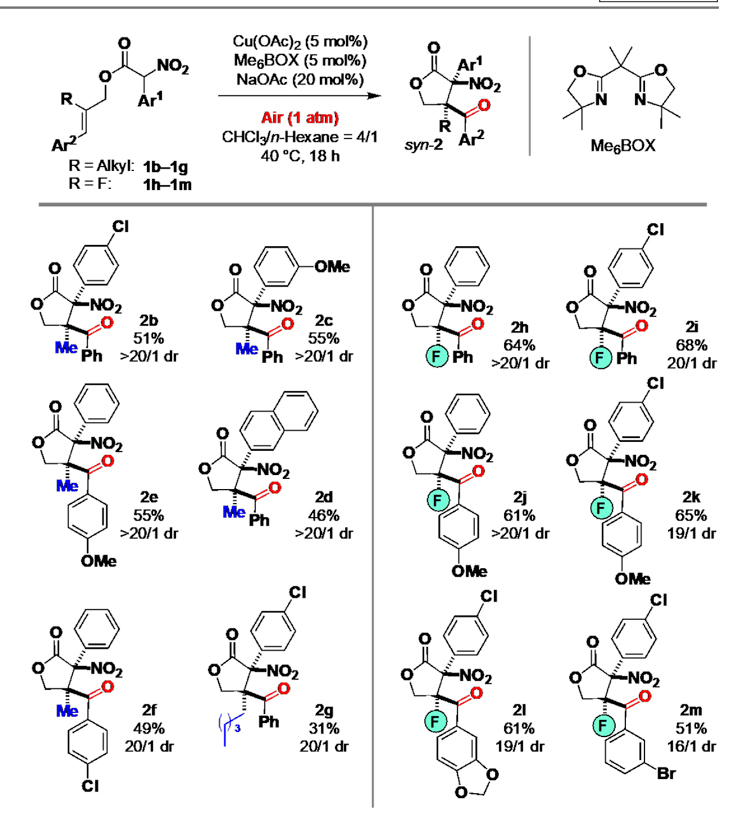 図3 空気中の酸素を酸化剤として用いるγ-ラクトンの触媒的合成
図3 空気中の酸素を酸化剤として用いるγ-ラクトンの触媒的合成
本研究で合成したさまざまな置換基を有するγ-ラクトン(2b-2m)。
反応条件を検証したところ、酢酸銅、Me6BOX配位子、および酢酸ナトリウムは、原料1aからラジカルを発生させるために重要であることが分かりました。さらには、原料1aからラジカルが発生すると、自発的に反応が進行することも示唆されました。そこで、生じたラジカルが分子内ラジカル環化においてどのようにsyn選択的に炭素–炭素結合を形成するのかを明らかにするために、密度汎(はん)関数計算[7]による解析を行いました(図4)。
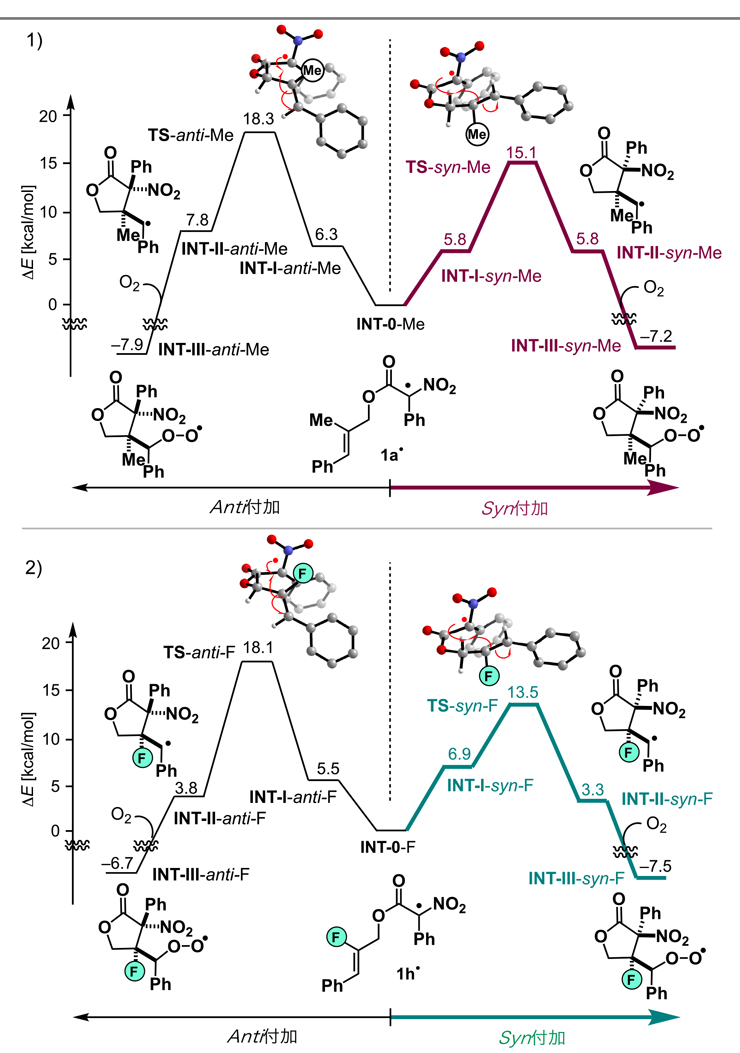 図4 密度汎関数計算による反応経路の解析
図4 密度汎関数計算による反応経路の解析
1)原系ラジカル「1a•」のラジカル環化/酸素付加。2)原系ラジカル「1h•」のラジカル環化/酸素付加。縦軸は反応経路におけるエネルギー(kcal/mol)を表す。
その結果、検証した全ての反応経路において、(1)環化後に生じるベンジルラジカル中間体INT-IIのエネルギーは原系ラジカルINT-0よりも高く、ラジカル環化過程は吸熱的であること、( 2)酸素がベンジルラジカル中間体INT-IIと速やかに反応することでより安定な生成物へと変換されること、が示されました。また、原系ラジカル「1a•」、「1h•」のいずれの反応経路においてもsyn体を与える遷移状態のエネルギー(TS-syn-Me:15.1 kcal/mol、TS-syn-F:13.5 kcal/mol)がanti体を与える遷移状態のエネルギー(TS-anti-Me:18.3 kcal/mol、TS-anti-F:18.1 kcal/mol)よりも小さいことが分かりました。これは前者が後者よりも反応速度が速く、選択的に起こることを意味します。
次に、syn体を与える遷移構造「TS-syn-Me」と「TS-syn-F」について、さらに解析を行いました(図5)。Baldwin則[8]に従うと、遷移構造において炭素ラジカルと二重結合の角度が109°のとき、軌道間相互作用が最も大きくなり理想的にラジカル付加が進行します。いずれの場合においても、炭素ラジカルと二重結合の角度(TS-syn-Me:107°、TS-syn-F:110°)は、理論値(109°)に近い値となりました。さらには、NBO(Natural Bond Orbital:自然結合軌道)解析[9]を行った結果、フッ素は電気陰性度が大きく、「C–F結合」は分極しているため、「TS-syn-F」は超共役効果(σC–H → σ*C–F)と水素結合(nF →σ*C–F)により安定化されることも明らかになりました(計16.6 kcal/mol)。これまでフッ素の超共役や水素結合は基底状態での立体配座[10]の安定化において主に議論されてきました。一方、これらの結果は、フッ素の超共役や水素結合が、反応の遷移状態エネルギーを小さくし、反応を促進することにも貢献できることを示しています。
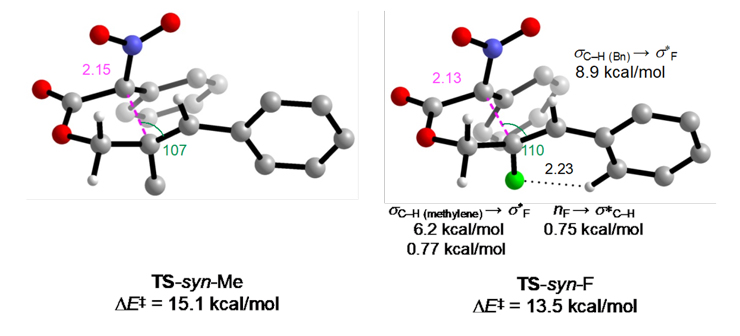 図5 遷移構造の解析
図5 遷移構造の解析
NBO解析で電子のドナー・アクセプター相互作用を算出した結果、TS-syn-Fは超共役(ドナー: C–Hの結合性軌道、アクセプター: C–Fの反結合性軌道)と水素結合(ドナー: Fの孤立電子対、アクセプター: C–Hの反結合性軌道)により、安定化されることが分かった(計16.6 kcal/mol)。
注)2020年10月22日プレスリリース「位置多様性・脱水素型クロスカップリング」
https://www.riken.jp/press/2020/20201022_1/index.html
今後の期待
共同研究グループは、空気中の酸素を用い、二つの連続四置換炭素を有するγ-ラクトンの合成を実現しました。得られる生成物はさまざまな分子に変換できることから、連続四置換炭素を持つ複雑分子の選択的供給に貢献すると期待できます。また計算化学を用いて、ラジカル環化反応で連続する二つの四置換炭素が構築される仕組みと、中間体として生じるベンジルラジカルを酸素で補足することでより安定なγ-ラクトン生成物へと変換されるユニークな連続反応プロセスを明らかにしました。これらの知見は、空気中の酸素を使う酸化的分子変換を開発するための有用な設計指針になると期待されます。
今回の研究は、国際連合が定めた17項目の「持続可能な開発目標(SDGs)[11]」のうち「12.つくる責任つかう責任」に貢献する成果です。
論文情報
- タイトル:Catalytic Aerobic Carbooxygenation for Construction of Vicinal Tetrasubstituted Centers: Application to the Synthesis of Hexa-substituted γ-Lactones
- 著者名:Florian Pünner, Yoshihiro Sohtome, Yanzong Lyu, Daisuke Hashizume, Mai Akakabe, Mami Yoshimura, Yoko Yashiroda, Minoru Yoshida, and Mikiko Sodeoka
- 雑誌:Angewandte Chemie International Edition
- DOI:10.1002/anie.202405876
補足説明
- [1] 四置換炭素
- 水素以外の四つの原子と結合した炭素のこと。四つの炭素原子と結合した炭素の四級炭素を含む。
- [2] γ-ラクトン
- 五員環の環状エステルの総称。炭素数をギリシア文字で表し、三員環はα-ラクトン、四員環はβ-ラクトン、五員環はγ-ラクトンと呼ぶ。
- [3] ラジカル
- 不対電子を持つ化学種の総称。通常、電子は二つずつ対になって存在し、安定な結合を形成する。熱や光により電子が励起されることによって不対電子ができ、ラジカルが発生する。構造式や化合物番号に「•」を付けて表す。
- [4] 持続性ラジカル
- 共役や立体効果により速度論的安定化を受け半減期が0.001秒より著しく長いラジカルの総称。一方、室温で単離できるほど長寿命のラジカルは安定ラジカル(長寿命ラジカル)と呼ぶ。
- [5] 反応性ラジカル(短寿命ラジカル)
- 半減期が0.001秒より著しく短いラジカルの総称。
- [6] ジェミナル二置換アルケン
- アルケンとは分子内に「C=C」の二重結合を含む不飽和炭化水素の総称。二つの炭素のうちどちらか一方に水素以外の二つの原子が結合したアルケンのことをジェミナル二置換アルケンと呼ぶ。ジェミナル(geminal)とは、同じ原子に結合する二つの置換基を指す。
- [7] 密度汎(はん)関数計算
- 原子や分子などの物性を明らかにする量子化学計算手法の一つ。反応が進行する際に最もエネルギーが高い状態を「遷移状態」と呼ぶ。遷移状態は、エネルギーが高く不安定なため実験的には観測は困難であるが、量子化学計算によりその構造を見ることができる。
- [8] Baldwin則
- Jack Edward Baldwinにより提唱された分子内求核反応の起こりやすさについての経験則。求電子反応およびラジカル反応にも適用することができる。
- [9] NBO(Natural Bond Orbital:自然結合軌道)解析
- 自然結合軌道とは、電子密度が最大となるように計算された結合性軌道のこと。自然結合軌道を解析することで、電子のドナー・アクセプター相互作用により得られる安定化エネルギーを定量できる。
- [10] 立体配座
- 単結合の回転により相互に変換可能な空間的な原子の配置のこと。
- [11] 持続可能な開発目標(SDGs)
- 2015年9月の国連サミットで加盟国の全会一致で採択された「持続可能な開発のための2030アジェンダ」にて記載された、2016年から2030年までの15年間で達成する国際目標。持続可能な世界を実現するための17のゴール、169のターゲットから構成され、発展途上国のみならず、先進国自身が取り組むユニバーサル(普遍的)なものであり、日本としても積極的に取り組んでいる(外務省ホームページから一部改変して転載)。SDGsはSustainable Development Goalsの略。
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業基盤研究(B)「タンパク質メチル化関連因子の化学的複合制御(研究代表者:五月女宜裕)」、同学術変革領域研究(B)「neo-PTMsの階層間シナジー(研究代表者:五月女宜裕)」による助成を受けて行われました。




